A faixa etária aprovada para a utilização de clonidina transdérmica é de 18 anos ou mais.Não está explicitamente aprovada para menores de 18 anos.O adesivo transdérmico de clonidina foi aprovado pela FDA em 1984 para o tratamento da hipertensão ligeira a moderada, isoladamente ou com um diurético, e funciona como um agente hipotensor alfa-agonista de ação central.
Pontos-chave explicados:
-
Restrição de idade aprovada pela FDA
- Clonidina transdérmica não é não está aprovado para doentes com menos de 18 anos .Esta restrição é repetida em várias referências, sublinhando a sua importância na utilização clínica.
- O adesivo é especificamente indicado para adultos (18+), provavelmente devido à insuficiência de dados de segurança/eficácia em populações pediátricas ou a potenciais riscos exclusivos dos doentes mais jovens.
-
Utilização médica primária
- Aprovado para tratar hipertensão ligeira a moderada (tensão arterial elevada), em monoterapia ou em associação com um diurético.
- O seu mecanismo consiste em atuar como um alfa-agonista de ação central que reduz a atividade do sistema nervoso simpático para baixar a pressão arterial.
-
Antecedentes regulamentares
- A FDA aprovou a formulação transdérmica em 1984 reflectindo o seu papel de longa data no tratamento da hipertensão.
- A limitação de idade manteve-se consistente desde a aprovação, sugerindo que não há evidências subsequentes para apoiar o uso pediátrico.
-
Considerações clínicas para os compradores
- Os prestadores de cuidados de saúde que compram o adesivo devem verificar a idade do doente para evitar a utilização não autorizada em crianças.
- A restrição implica que podem ser necessárias terapêuticas anti-hipertensivas alternativas para os doentes pediátricos.
Esta clareza garante o cumprimento das diretrizes de prescrição e a segurança dos doentes.Para as populações adultas, o adesivo oferece uma opção não oral para o controlo da tensão arterial - um pormenor valioso para os decisores de fórmulas.
Tabela de resumo:
| Aspeto-chave | Detalhes |
|---|---|
| Faixa etária aprovada | 18 anos ou mais (não para uso pediátrico) |
| Utilização primária | Tratamento da hipertensão ligeira a moderada |
| Mecanismo de ação | Alfa-agonista de ação central para baixar a pressão arterial |
| Ano de aprovação pela FDA | 1984 |
| Considerações clínicas | Verificar a idade do paciente; são necessárias terapias alternativas para pacientes com menos de 18 anos |
Precisa de soluções transdérmicas fiáveis para o tratamento da hipertensão em adultos?
A Enokon é especializada no fabrico a granel de adesivos transdérmicos de alta qualidade, incluindo formulações de clonidina, para distribuidores de cuidados de saúde e marcas farmacêuticas.A nossa experiência garante a conformidade com as diretrizes da FDA e uma integração perfeita na sua linha de produtos.
Contacte-nos hoje para falar sobre I&D personalizada, encomendas em massa ou apoio regulamentar - vamos melhorar os cuidados dos doentes em conjunto.
Guia Visual
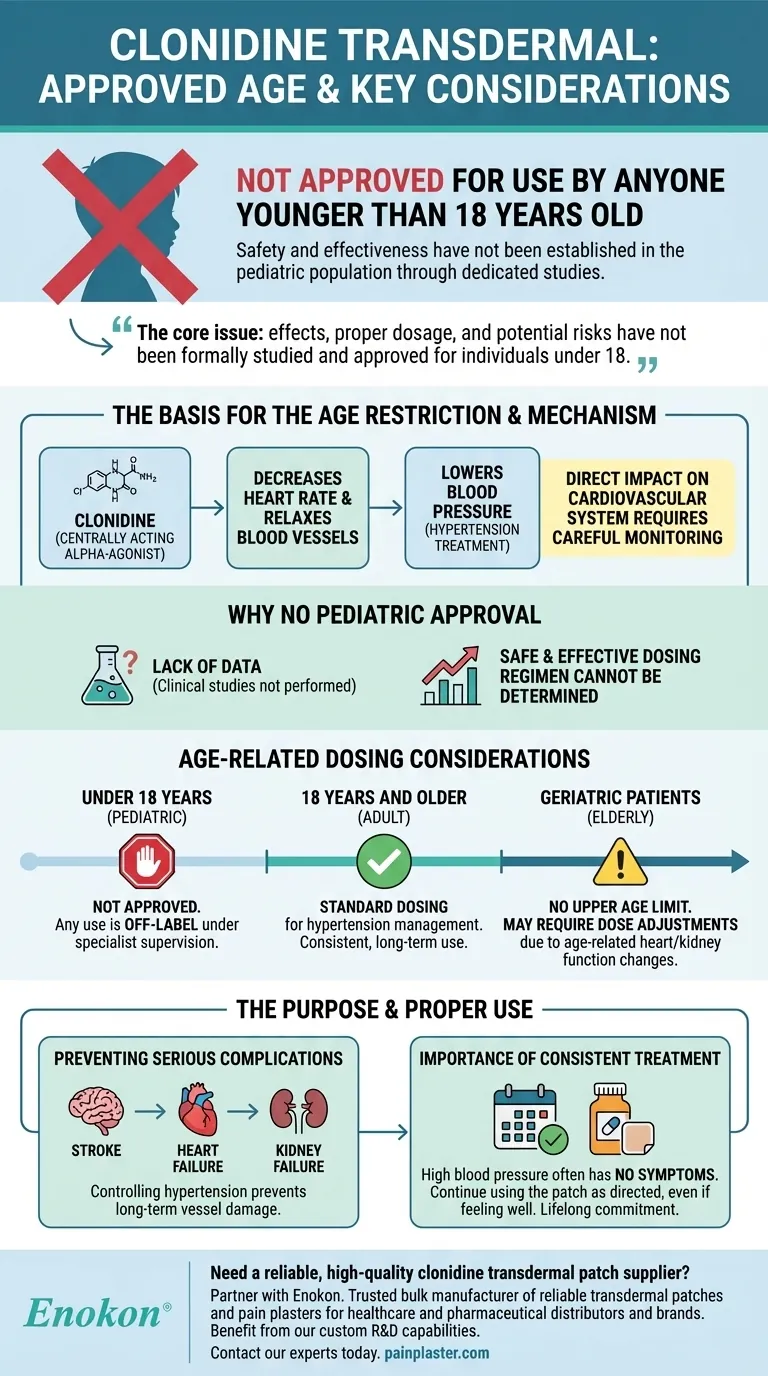
Produtos relacionados
- Patches de calor infravermelho distante para alívio da dor Patches transdérmicos
- Patch de silicone para cicatrizes Patch transdérmico para medicamentos
- Patch de alívio da dor Icy Hot Menthol Medicine
- Patch de alívio da dor em gel de mentol
- Patch de alívio da dor de absinto para dores no pescoço
As pessoas também perguntam
- Que papel os adesivos transdérmicos desempenham na melhoria das lesões cutâneas? Descubra como a estabilização previne as úlceras de pressão
- Qual o papel de um dessecador na análise do teor de umidade de adesivos transdérmicos? Garanta Estabilidade e Segurança
- Que factores influenciam a eficácia dos adesivos transdérmicos?Considerações fundamentais para uma administração óptima de medicamentos
- Quais são as desvantagens da administração transdérmica de medicamentos?Principais limitações a considerar
- Como é que os adesivos transdérmicos melhoram a adesão à medicação?Aumentar a adesão ao tratamento com facilidade











