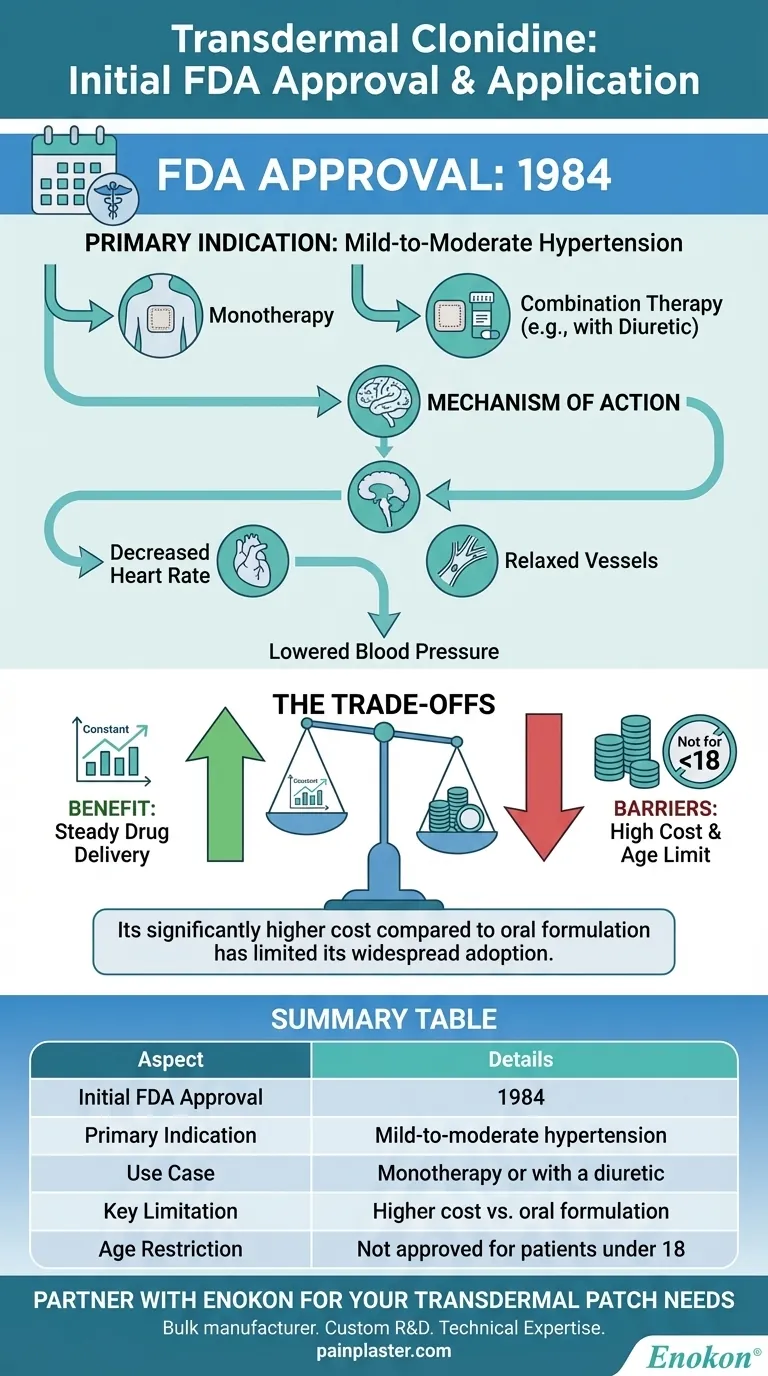
A clonidina transdérmica foi inicialmente aprovada pela Food and Drug Administration (FDA) dos EUA em 1984 para o tratamento da hipertensão ligeira a moderada, quer como terapia autónoma quer em combinação com um diurético.Esta aprovação marcou a introdução de um novo método de administração da clonidina, aproveitando a sua capacidade de baixar a tensão arterial através de mecanismos alfa-agonistas centrais.O adesivo transdérmico oferecia vantagens como a libertação sustentada do fármaco e a melhoria da adesão do doente, o que, na altura, constituiu um avanço significativo no tratamento da hipertensão.
Pontos-chave explicados:
-
Aprovação inicial da FDA (1984)
- O adesivo transdérmico de clonidina recebeu a aprovação da FDA em 1984, especificamente para o tratamento da hipertensão ligeira a moderada.
- Esta aprovação validou a sua eficácia como monoterapia ou como adjuvante de diuréticos, respondendo a uma necessidade crítica de opções anti-hipertensivas de ação prolongada.
-
Indicação primária:Hipertensão
-
O adesivo foi concebido para fornecer clonidina de forma contínua, reduzindo a tensão arterial ao
- Diminuição do ritmo cardíaco.
- Relaxamento dos vasos sanguíneos para melhorar a circulação.
- A sua classificação como um agente hipotensor alfa-agonista de ação central sublinha o seu mecanismo de ação no tronco cerebral para modular o fluxo simpático.
-
O adesivo foi concebido para fornecer clonidina de forma contínua, reduzindo a tensão arterial ao
-
Vantagens da administração transdérmica
- Ao contrário das formulações orais, o adesivo assegura níveis estáveis de fármaco, minimizando as flutuações entre o pico e o vale.
- A frequência de dosagem reduzida (por exemplo, aplicação semanal) aumentou a adesão, particularmente para doenças crónicas como a hipertensão.
-
Restrições de idade
- Nomeadamente, a forma transdérmica não foi aprovada para doentes com menos de 18 anos, reflectindo dados de segurança limitados em populações pediátricas na altura.
-
Contexto histórico
- A aprovação de 1984 representou uma inovação na administração de medicamentos, alinhando-se com as tendências mais amplas de terapias não orais para doenças cardiovasculares.
- Complementou a clonidina oral existente, oferecendo uma alternativa para os doentes com problemas de tolerabilidade gastrointestinal.
O adesivo transdérmico de clonidina continua a ser um testemunho da forma como os sistemas de administração de fármacos direcionados podem transformar a gestão de doenças crónicas - optimizando silenciosamente a terapia através de uma ciência que vai até à pele.
Tabela de resumo:
| Aspeto-chave | Detalhes |
|---|---|
| Ano de aprovação da FDA | 1984 |
| Indicação primária | Hipertensão ligeira a moderada (em monoterapia ou com diuréticos) |
| Mecanismo de ação | Alfa-agonista de ação central, reduz o fluxo simpático |
| Principais vantagens | Libertação estável do fármaco, melhor conformidade, dosagem semanal |
| Restrições de idade | Não aprovado para pacientes com menos de 18 anos |
Precisa de soluções transdérmicas fiáveis para a hipertensão ou para a dor crónica?
A Enokon é especializada em adesivos transdérmicos de alta qualidade, combinando décadas de experiência com P&D personalizável para marcas e distribuidores farmacêuticos.
Contacte-nos hoje
para discutirmos o seu projeto - vamos inovar juntos!
Guia Visual
Produtos relacionados
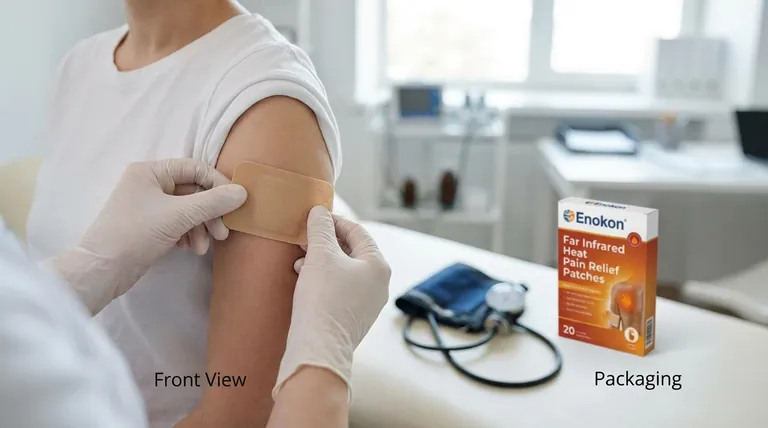
- Patch de alívio da dor em gel de mentol
- Patch de silicone para cicatrizes Patch transdérmico para medicamentos
- Patches de calor infravermelho distante para alívio da dor Patches transdérmicos
- Patch de alívio da dor Icy Hot Menthol Medicine
- Patch de alívio da dor de absinto para dores no pescoço
As pessoas também perguntam
- Quem deve consultar um profissional de saúde antes de utilizar pensos para alívio da dor?Guia de segurança
- Qual a eficácia dos pensos analgésicos para as dores musculares?Alívio direcionado sem efeitos secundários sistémicos
- Quando é que deve considerar a utilização de produtos para o alívio da dor, como cremes e adesivos?Otimizar o conforto e a segurança
- Quais são algumas das aplicações comuns dos pensos para alívio da dor?Alívio direcionado para o controlo da dor
- Quais são os diferentes tipos de adesivos para alívio da dor disponíveis?Encontre a solução certa para a sua dor




