A toxicidade dos adesivos transdérmicos é monitorizada através de uma combinação de estudos pré-clínicos de irritação da pele, modelos preditivos e vigilância pós-comercialização.Os métodos primários incluem o teste do Índice de Irritação Primária (PII) para avaliar reacções cutâneas localizadas, como eritema e edema, juntamente com modelos computacionais que analisam as interações fármaco-pele.Os protocolos de eliminação adequados são essenciais para evitar riscos de exposição secundária.Estas abordagens em camadas garantem a segurança desde o desenvolvimento até à utilização no mundo real.
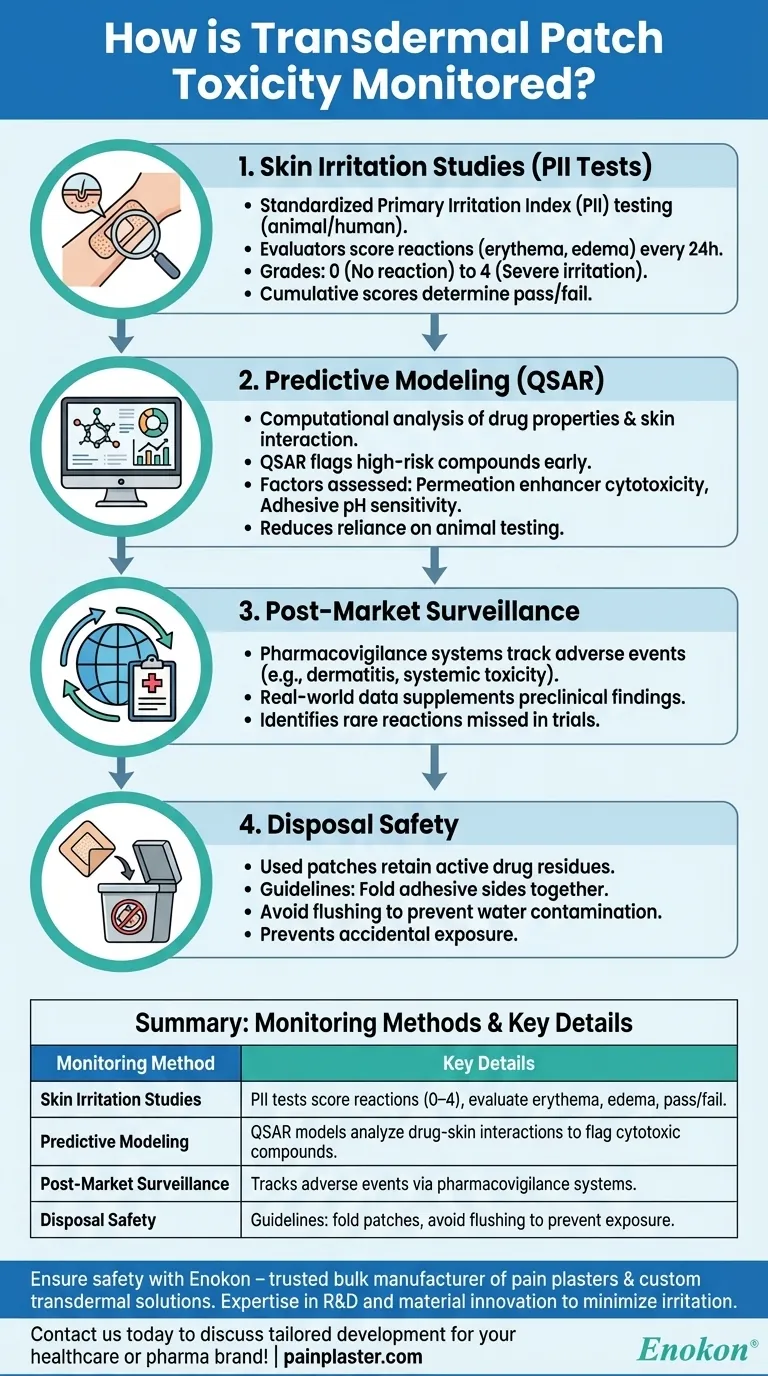
Pontos-chave explicados:
-
Estudos de Irritação da Pele (Testes PII)
- O adesivo transdérmico é submetido a testes padronizados do Índice de Irritação Primária (PII), em que os adesivos são aplicados na pele animal ou humana em condições controladas.
-
Os avaliadores classificam as reacções (vermelhidão, inchaço) em intervalos de 24 horas, com graus:
- 0 (sem reação) a 4 (irritação grave).
- As pontuações acumuladas determinam os limiares de aprovação/reprovação para desenvolvimento posterior.
-
Modelação preditiva
- As ferramentas computacionais analisam as propriedades dos medicamentos (por exemplo, solubilidade, peso molecular) e a sua interação com as camadas da pele.
- Modelos como o QSAR (Relação Quantitativa Estrutura-Atividade) identificam precocemente compostos de alto risco, reduzindo a dependência de ensaios em animais.
-
Factores avaliados:
- Citotoxicidade dos potenciadores de permeação química.
- Sensibilidade ao pH das camadas adesivas.
-
Vigilância pós-comercialização
- Os sistemas de farmacovigilância acompanham os acontecimentos adversos (por exemplo, dermatite de contacto, toxicidade sistémica) comunicados pelos prestadores de cuidados de saúde ou pelos doentes.
- Os dados do mundo real complementam os resultados pré-clínicos, identificando reacções raras que não foram detectadas nos ensaios.
-
Segurança da eliminação
- Os pensos usados retêm resíduos de fármacos activos; a eliminação incorrecta acarreta o risco de exposição acidental (por exemplo, crianças/animais de estimação).
-
As diretrizes incluem:
- Dobrar os lados do adesivo antes da eliminação.
- Evitar a lavagem para prevenir a contaminação da água.
-
Tecnologias emergentes
- As matrizes de microagulhas e os materiais biodegradáveis têm como objetivo reduzir os riscos de irritação e, ao mesmo tempo, aumentar a precisão da administração do medicamento.
Ao integrar estas estratégias, os fabricantes equilibram a eficácia com a segurança do doente, garantindo que os pensos cumprem as normas regulamentares e minimizam os danos.Já pensou em como as inovações de materiais podem reduzir ainda mais a irritação em designs futuros?
Tabela de resumo:
| Método de controlo | Detalhes principais |
|---|---|
| Estudos de Irritação da Pele | Os testes PII classificam as reacções (0-4) para avaliar o eritema, o edema e os limiares de aprovação/reprovação. |
| Modelação preditiva | Os modelos QSAR analisam as interações fármaco-pele para identificar precocemente os compostos citotóxicos. |
| Vigilância pós-comercialização | Acompanha os acontecimentos adversos (por exemplo, dermatite) através de sistemas de farmacovigilância. |
| Segurança na eliminação | As diretrizes incluem dobrar os pensos e evitar a descarga para evitar a exposição. |
Assegure-se de que os seus adesivos transdérmicos cumprem as normas de segurança com o Enokon -o seu fabricante de confiança de pensos analgésicos fiáveis e soluções transdérmicas personalizadas.A nossa experiência em I&D e inovação de materiais ajuda a minimizar os riscos de irritação e a maximizar a eficácia. Contacte-nos hoje para discutir o desenvolvimento personalizado para a sua marca de cuidados de saúde ou farmacêutica!
Guia Visual
Produtos relacionados
- Patch de silicone para cicatrizes Patch transdérmico para medicamentos
- Patches de calor infravermelho distante para alívio da dor Patches transdérmicos
- Patch de alívio da dor em gel de mentol
As pessoas também perguntam
- Quais são os efeitos adversos mais comuns da administração transdérmica de medicamentos?Riscos e dicas de prevenção
- Como um molde coberto ou funil invertido afeta a evaporação do solvente em adesivos transdérmicos? Otimize a Qualidade do Filme.
- Quais são os principais benefícios dos sistemas de administração transdérmica de medicamentos?Melhorar o tratamento com precisão e comodidade
- Quais são as vantagens dos adesivos transdérmicos?Otimizar a administração de medicamentos com pensos
- Onde é que os utilizadores podem encontrar mais informações sobre a segurança dos adesivos?Recursos essenciais para uma utilização segura


